近日,中国医学科学院药物研究所王锐院士团队在化学顶尖期刊《美国化学会志》(Journal of the American Chemical Society),在线发表题为“Triazination/IEDDA Cascade Modular Strategy Installing Pyridines/Pyrimidines onto Tyrosine Enables Peptide Screening and Optimization”(三嗪化/IEDDA级联模块化策略将吡啶/嘧啶安装到酪氨酸上以实现多肽筛选与优化)的研究论文,并被选为增选封面Supplementary Cover。
多肽药物凭借其高靶向性和低毒性成为生物医药领域的研究热点,但其临床应用长期受限于体内稳定性差、膜渗透性低等固有缺陷。传统模块化修饰策略依赖于预先引入非天然氨基酸,不仅增加了合成复杂性,还因固定连接方式限制了分子多样性。针对这一难题,王锐院士团队提出创新性解决方案——酪氨酸-1,2,3-三嗪连接策略(Tyrosine-Triazine-Ligation, YTL)。该策略通过结合SNAr和IEDDA反应的“一锅两步”过程构建新的连接(吡啶和嘧啶),促进含Tyr肽的模块化后修饰,为多肽结构的多样性提供了新的可能,并在抗菌短肽成药性优化中得到了验证和应用。该策略简单、高效、实用,反应模块商业可得或制备简单,完美契合模块化后修饰的需求。
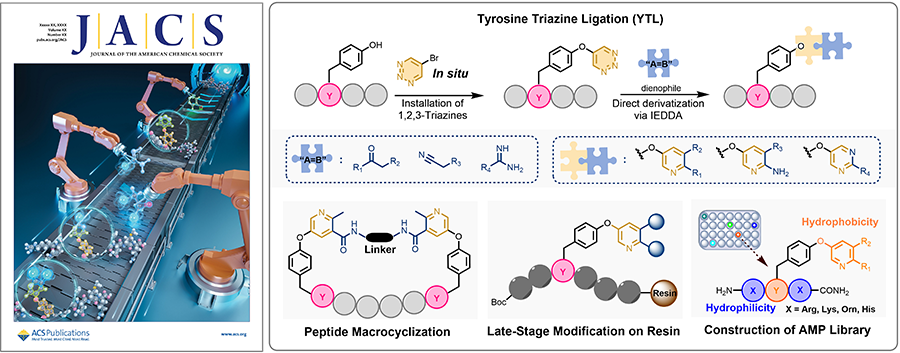
研究发现,YTL策略展现出高度的灵活性,不仅可兼容多种亲二烯模块,还能实现多肽环化。为验证YTL策略在多肽药物固相修饰中的应用潜力,该团队在固相条件下,实现了系列生物活性多肽的精准修饰。首先,作者以穿膜肽TAT作为模式肽,通过YTL策略实现了N端DOTA和酪氨酸侧链FITC的双修饰,构建了荧光素/核素双模成像探针T3,通过激光共聚焦和流式细胞术实验,证明了其应用价值。其次,利用YTL策略实现了对GLP-1分子的精准修饰,引入PEG-脂肪酸链显著延长了半衰期。特别是,团队基于该策略,利用96孔板高通量构建了包含384种化合物的抗菌肽库,从中筛选出高活性核心序列RYR,并进一步优化出兼具选择性与杀菌效力的稳定多肽Z8,充分展现了该策略在药物筛选和优化中的高效性。
综上,本研究创新性地开发了YTL策略,为高通量多肽合成、筛选和优化提供了一个多功能、高效的平台。团队目前正将这一策略应用于多肽核药的从头筛选中,以加速多肽药物从实验室到临床的转化进程。
药物所王锐院士,胡宽研究员,兰州大学孙旺盛青年教授为本文共同通讯作者。药物所“协和青年学者”博士后左权(药物所2024届博士),以及兰州大学硕士生宋昕旖和药物所硕士生闫洁为本文共同第一作者。该工作得到了中国医学科学院医学与健康科技创新工程(2021-I2M-1026、2021-I2M-3-001、2023-I2M-2-006、2023-I2M-M-QJ-010、2024-I2M-ZH-009)、中央高校基本科研业务费专项资金(lzujbky-2024-ey10)、国家自然科学基金(22307052、82372002)、中国医学科学院多肽创新单元(IRT_15R27)和中国医学科学院中央级公益性科研院所基本科研业务费基金(2022RC350-04)的资助。
论文链接:https://doi.org/10.1021/jacs.4c17615

