近期,中国医学科学院药物研究所王锐院士团队在PD-L1靶向肽类放射性药物研发领域接连取得重要突破,相关成果分别发表于《Journal of the American Chemical Society》与中科院一区Top期刊《Journal for ImmunoTherapy of Cancer》。两项研究从不同维度展示了肽类核药的结构优化策略,为肿瘤PD-L1靶点显像与联合治疗提供了新的思路。
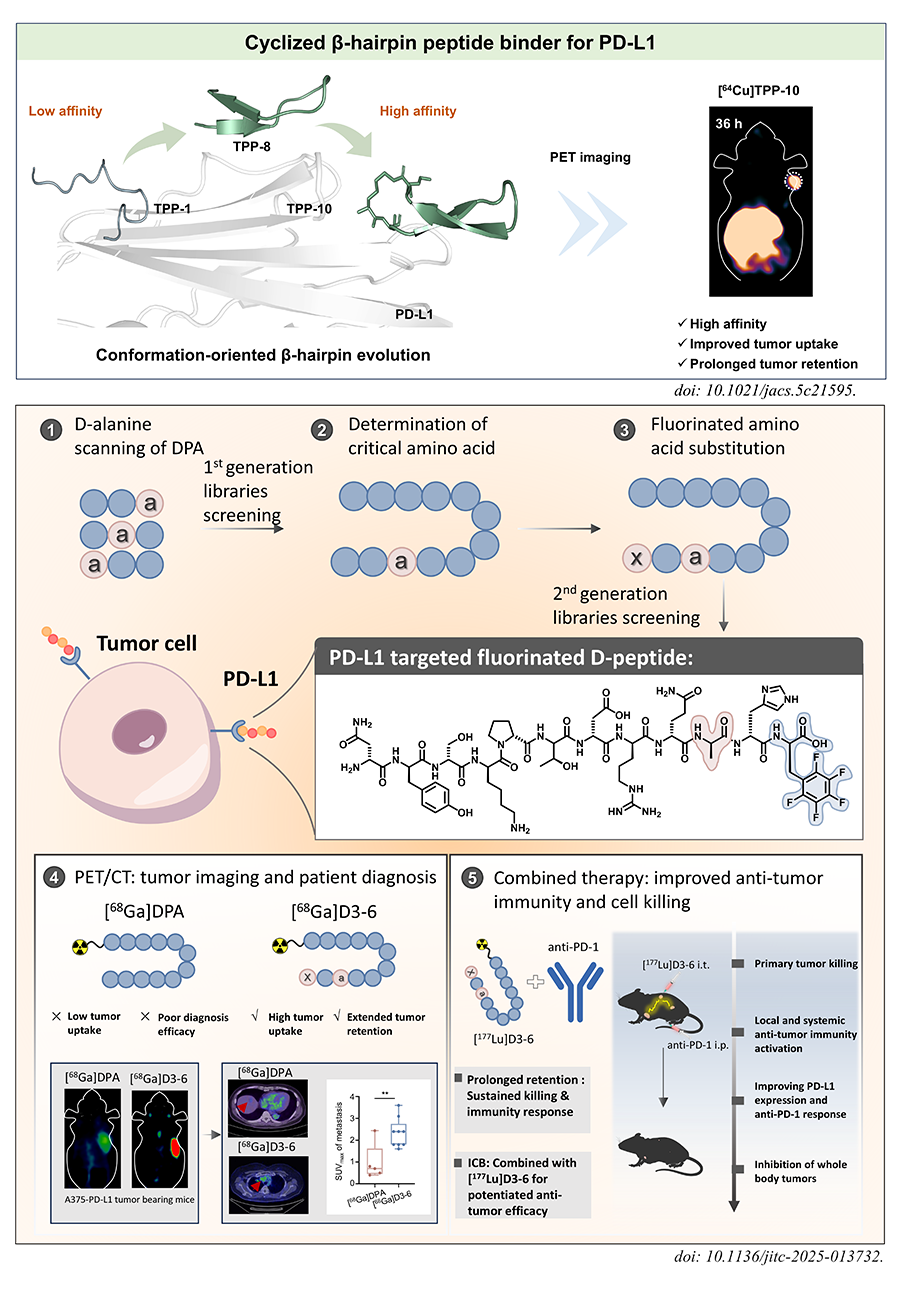
团队针对PD-L1/PD-1 β-hairpin相互作用界面平坦、难以开发高亲和力肽配体的挑战,探索了β-发夹构象定向工程策略。以已知线性肽TPP-1为起点,通过多轮化学改造逐步“锁定”构象,获得环状β-发夹肽TPP-10。圆二色光谱、核磁共振及小角X射线散射等多维度结构验证表明,TPP-10形成高度稳定的β-发夹结构。经过[68Ga]与[64Cu]标记后,PET显像显示其在荷瘤小鼠中肿瘤摄取与滞留时间显著提升,使用半衰期更长的64Cu标记时,显像可持续至36小时,肿瘤/肌肉比值达9.08,成像对比度与靶向特异性显著提高。
与此同时,团队针对PD-L1靶点,聚焦于D-肽的体内性能优化。传统L-肽易被酶解、肿瘤滞留不足,限制了其在放射配体疗法中的应用。研究团队通过氟化修饰策略,在前期D-肽DPA基础上,经D-丙氨酸扫描与氟代氨基酸筛选,获得五氟修饰的D-苯丙氨酸取代的优化分子D3-6,[68Ga]D3-6在荷瘤小鼠模型中4小时摄取达到22.43±1.63%ID/g,显著优于母体分子;初步临床研究进一步验证了其诊断价值,[68Ga]D3-6在肿瘤原发灶以及转移灶的检测率达100%,而对照分子[68Ga]DPA检出率为20%,显示出优异的诊断效率。治疗性核药[177Lu]D3-6联合anti-PD-1免疫治疗,不仅有效抑制原发肿瘤,还增强CD8⁺ T细胞效应功能及促进M1型巨噬细胞极化,激活系统性抗肿瘤免疫,实现远端肿瘤抑制。该策略将氟化修饰与D-肽稳定性优势相结合,为提升放射配体疗法与免疫联合治疗疗效提供了可行路径。
两项工作分别从不同角度出发提高多肽PD-L1靶向性能:一方面从构象出发,通过β-发夹构象“锁定”稳定二级结构,有效提升多肽亲和力与体内药代动力学行为。另一方面,从理化性质调控出发,通过氟化修饰增强亲和力与膜穿透性,提高了D-肽的肿瘤蓄积。两种策略为PD-L1靶向诊疗一体化探针的临床转化奠定了重要基础,也为其他由β-折叠界面介导的难成药相关靶点的核药开发提供了可推广的范式。
王锐院士以及胡宽研究员为两篇文章的共同通讯作者,助理研究员张思琪、硕士研究生刘灿为两篇文章的共同第一作者。两项研究获得国家自然科学基金(82372002、82502399、22507148)与中国医学科学院医学与健康科技创新工程(2024-I2M-ZH-009、2023-I2M-2-006、2025-I2M-XHJC-026、2025-I2M-XHXX-026)等项目支持。
论文链接:
https://doi.org/10.1021/jacs.5c21595
https://doi.org/10.1136/jitc-2025-013732