2022年7月7日,中国医学科学院药物研究所“天然药物活性物质与功能”国家重点实验室蒋建东院士、王琰研究员为共同通讯作者,与吉林大学心血管中心佟倩教授合作在国际著名期刊Signal Transduction and Targeted Therapy(影响因子38.1)在线发表了“Berberine treats atherosclerosis via a vitamine-like effect down-regulating Choline-TMA-TMAO production pathway in gut microbiota”论文,首次阐明了小檗碱(BBR)以维生素样的作用下调肠道菌胆碱-TMA-TMAO代谢通路而改善动脉粥样硬化症的分子机制。
心血管疾病(CVD)是当前人类死亡的首要原因,而动脉粥样硬化(AS)是CVD的病理基础。AS的发病机制有多种危险因素和分子机制,如高血脂或高血糖、局部或全身炎症反应等。近年来,越来越多的证据表明,肠道菌是AS发展和恶化的影响因素。其中,三甲胺(TMA)是一种肠道菌衍生的代谢产物,通过分解摄入的红肉或动物内脏中的膳食磷脂酰胆碱/胆碱、左旋肉碱或甜菜碱而生成。被吸收入血的肠道TMA被黄素单加氧酶家族成员(例如肝脏中的黄素单加氧酶3,FMO3)进一步转化为三甲胺-N-氧化物(TMAO),促进了AS斑块形成。最近的研究表明,与传统的危险因素不同,TMAO是AS的独立预测因子和促进剂。事实上,TMAO通过多种机制加重AS,包括增强对泡沫细胞形成的作用、血小板高反应性和血栓形成风险、直接激活炎症反应和干扰胆固醇的反向转运,因此,抑制肠道菌TMAO的生成被认为是干预AS疾病发生发展潜在的新靶点。
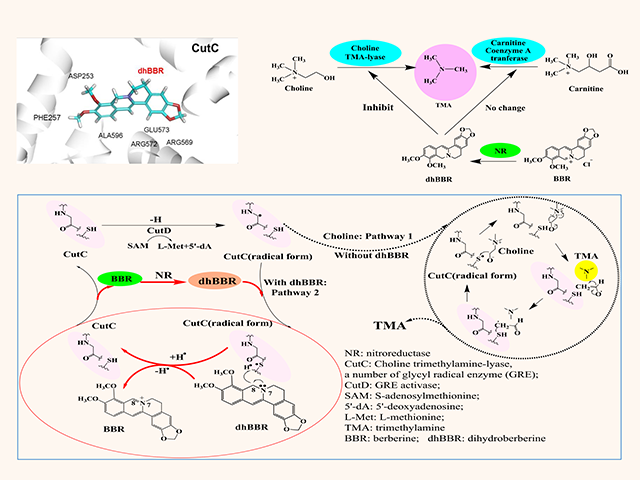
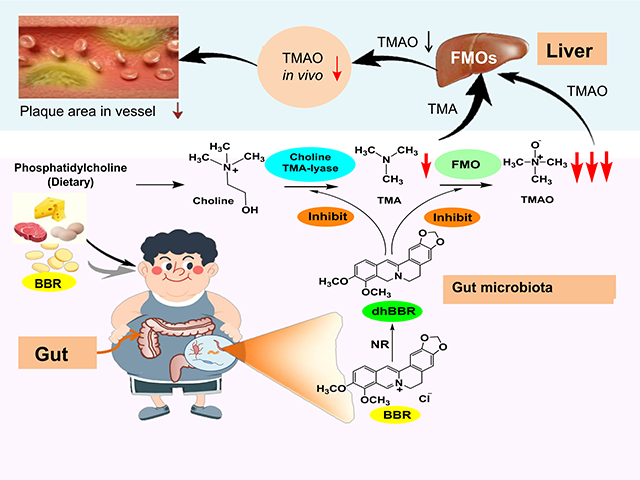
该研究首次揭示了AS金黄地鼠口服BBR降低了肠道中TMAO的生物合成。这种独特分子机制是通过小檗碱的代谢产物二氢小檗碱(dhBBR,一种肠道菌NR产生的还原型小檗碱)作用于肠道菌胆碱三甲胺裂解酶及辅酶(CutC/CutD)从而抑制了胆碱向TMA的转化;同时,dhBBR也作用于肠道菌黄素单加氧酶及辅酶(FMO/FAD),使TMA向TMAO转化被抑制,而dhBBR被氧化生成BBR。dhBBR与BBR相互转化,与维生素的作用方式相似(如维生素C与脱氢维生素C),最终下调了胆碱-TMA-TMAO代谢通路而改善AS。该研究也进一步开展了临床21个高脂血症伴AS患者口服BBR的试验,结果表明口服BBR四个月后斑块评分减少了3.2% (*P < 0.05),其粪便和血中TMA 和TMAO 含量分别降低了38%和 29%(粪便:*P < 0.05; *P < 0.05), 及37%和 35%(血:***P < 0.001; *P < 0.05)。结果证实,BBR可能作用于肠道菌CutC/CutD 及FMO/FAD并以维生素样的作用方式减少肠道菌TMAO的生物合成,从而改善AS。本文是首次发现小檗碱通过作用肠道菌NR-CutC/CutD-FMO酶系改善AS的药效及分子机制,并通过临床试验得到验证。该研究对天然药物(难吸收)体内代谢及分子药理的研究具有广泛的意义和重要的科学价值。
中国医学科学院医学与健康科技创新工程(No.2016-I2M-3-011,2021-I2M-1-007),NSFC(No. 81573493,82173888)和“创新药物非临床药物代谢及PK-PD研究”北京市重点实验室(Z141102004414062)等资助了该研究。马殊荣(2016级直博生)、佟倩(吉林大学第一医院心血管中心,教授)、林媛副研究员、潘利斌(2017级直博生)和符洁助理研究员为共同第一作者。
原文链接:https://www.nature.com/articles/s41392-022-01027-6

