10月18日,国际顶级化学期刊Angewandte Chemie International Edition(《德国应用化学》)在线发表了药物所戴均贵团队题为“Four Cytochrome P450 Enzymes Mediate Oxidation Cascades in the Biosynthesis of Cephalotane-Type Diterpenoids”(“四个细胞色素P450酶介导三尖杉烷型二萜生物合成中的氧化级联反应”)的研究论文。该研究是继报道三尖杉烷型二萜骨架形成的关键酶—三尖杉烯合酶(CsCTS)(Angew. Chem. Int. Ed. 2023, 62, e202306020)后,发现并功能鉴定了参与三尖杉烷型二萜结构中特征性的13,17-内酯、5,19-内酯和环庚三烯酮结构单元的4个P450氧化酶,首次完整解析了海南粗榧内酯醇(hainanolidol)等三尖杉烷型二萜的生物合成途径,并结合一步化学反应完成了海南粗榧内酯(harringtonolide)的合成。
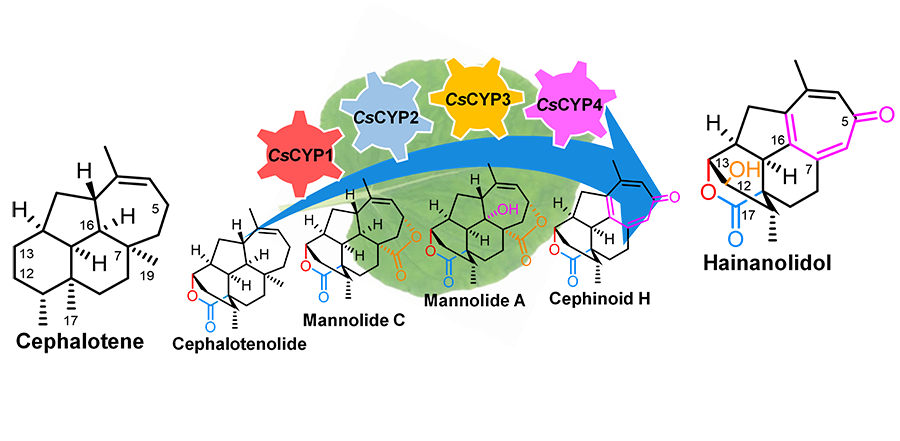
图. 4个CYP450酶(CsCYP1−CsCYP4)催化合成海南粗榧内酯醇
海南粗榧内酯是三尖杉属(Cephalotaxus)植物中三尖杉烷型(cephalotane-type)二萜的代表性成分,结构新颖独特,具有刚性骈合6/6/5/7四环二萜骨架,包含一个环庚三烯酮环、一个六元内酯桥环和一个四氢呋喃环及7个手性中心。药理学研究揭示其具有多种生物活性,尤其对人KB细胞的IC50值达43 nM,极具研发前景。但该化合物在植物中含量极低(~0.0009%),且结构复杂,化学合成难度大,导致其来源严重受限,通过生物合成方式获取有望为解决该难题提供新策略。前期研究中,戴均贵教授团队发现并功能鉴定了三尖杉烷型二萜骨架形成酶CsCTS,明确了该类化合物的基本骨架为三尖杉烯,并阐明了其环化机制。然而,将三尖杉烯进一步转化为海南粗榧内酯所涉及的后修饰步骤,包括特征性六元内酯桥环、呋喃环及环庚三烯酮等结构单元的形成及其相关后修饰酶仍然未知。
该研究利用共表达分析策略,以CsCTS为诱饵基因,筛选出具有较高共表达相关性的细胞色素P450基因,并在本氏烟草(Nicotiana benthamiana)中与二萜合酶CsCTS瞬时共表达进行功能分析。通过共表达产物的结构鉴定及底物饲喂,证实CsCYP1可催化三尖杉烯C-13羟基化、CsCYP2可连续氧化三尖杉烯17-Me生成17-ol和17-aldehyde产物,CsCYP1和CsCYP2可组合催化三尖杉烯生成13,17-内酯结构单元,完成海南粗榧内酯结构中的六元内酯桥环的合成。CsCYP3是一个多功能氧化酶,可催化三尖杉烯C-5、C-19和C-12等多位点的氧化,主要完成三尖杉烷型二萜结构中5,19-内酯结构单元合成。CsCYP4可催化mannolide C的C-16羟基化,介导了环庚三烯酮结构单元的形成。进一步将CsCYP1~CsCYP4与CsCTS在本氏烟草中共表达,成功合成了海南粗榧内酯直接前体海南粗榧内酯醇,随后,通过一步化学反应完成了海南粗榧内酯的合成。
该研究发现并鉴定了海南粗榧内酯等三尖杉烷型二萜生物合成过程的4个P450酶,通过协同催化氧化级联反应,催化基本骨架结构三尖杉烯生成三尖杉烷型二萜结构中特征性的13,17-内酯、5,19-内酯及环庚三烯酮结构单元,并在本氏烟草中实现了海南粗榧内酯直接前体海南粗榧内酯醇的合成。这些研究结果为理解并完整解析该类化合物生物合成途径提供了实验依据,也为通过生物合成或化学−生物合成策略实现海南粗榧内酯等三尖杉烷型二萜的绿色高效合成、解决其资源短缺问题及推动其新药研发奠定基础。
中国医学科学院药物研究所天然药物及核药基础与新药创制全国重点实验室、卫健委天然产物生物合成重点实验室、医科院酶与天然药物生物催化重点实验室、创新药物非临床药物代谢及PK/PD研究北京市重点实验室2021级博士生郭奥博和助理研究员刘继梅为论文第一作者,戴均贵、陈日道研究员及刘继梅博士为论文共同通讯作者。该项目得到了国家重点研发计划项目(2023YFA0914100)、国家自然科学基金项目(82473816、82550003和82422075)及医科院医学与健康科技创新工程(CIFMS-2024-I2M-TS-013)支持。感谢北京大学药学院徐正仁教授对环庚三烯酮环形成机制推测的帮助。
论文链接:https://doi.org/10.1002/anie.202512854